L’ASH a également permis de présenter de nouveaux résultats sur les prises en charge globale des patients : quand faire un myélogramme dans le bilan de pic monoclonal, faut-il continuer l’alimentation protégée dans les greffes de moelle osseuse, Comment évaluer le risque thrombotique artérielle et veineux dans les syndromes myéloprolifératifs ?
ASH 2022 – Résumé sur les traitements additionnels



Quand faire un myélogramme dans le bilan de pic monoclonal ?
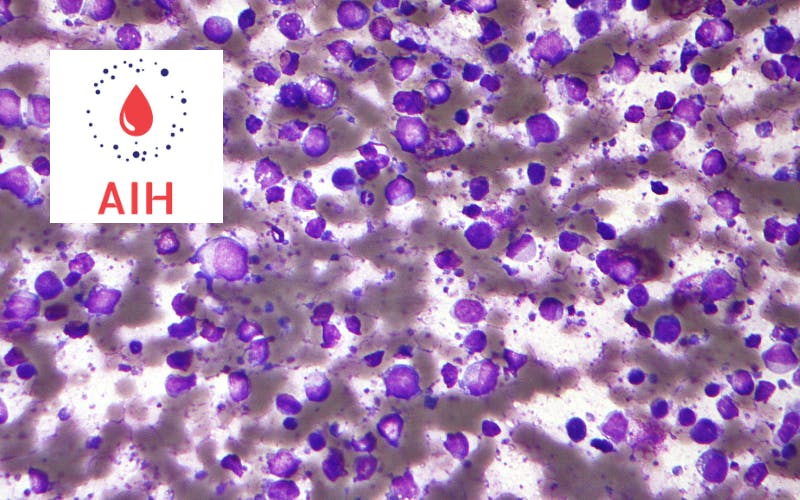
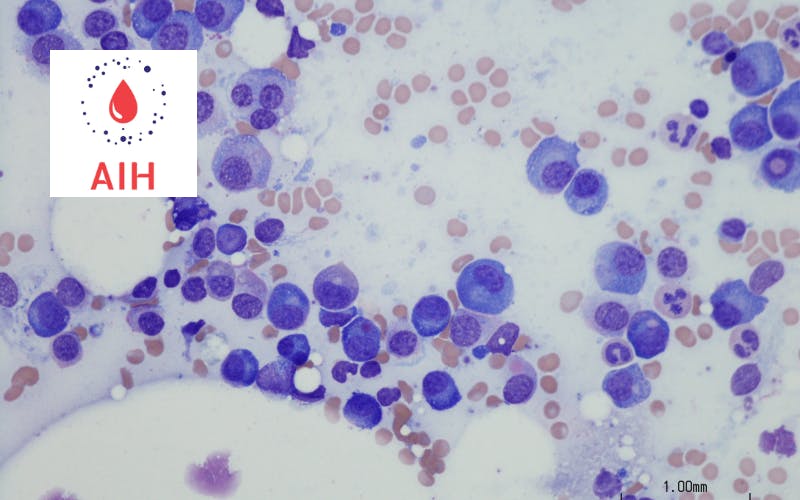
L’étude iStopMM (cohorte islandaise ayant recherché des gammapathies monoclonales dans la moitié de la population islandaise) a apporté de nombreux résultats épidémiologiques dont le plus intéressant concernant l’indication de myélogramme dans les pics monoclonaux sans manifestation clinique basé sur plus de 1000 patients. Ce myélogramme a pour but de différencier les MGUS(forme pré-cancer du sang, qui nécessite une surveillance annuelle) d’un myélome indolent qui nécessite une surveillance plus rapprochée tous les 6 mois. La présence d’une infiltration de cellules malades au niveau de la moellesigne lediagnostic de myélome indolent mais il est présent que dans 10% des cas. Dans ce contexte, 90% des patients doivent avoir un myélogramme sans impact thérapeutique direct. Eythorsson et son équipe proposent un score pour sélectionner les patients ayant une probabilité plus forte d’avoir un myélome indolent grâce des scores de biologies sanguines plus simple à obtenir. Grâce au score, deux tiers des patients peuvent éviter le myélogramme lors de la prise en charge initiale. Une cohorte de validation sera nécessaire pour valider ce score. Le calculateur est maintenant disponible.
Faut il continuer l’alimentation protégée dans les greffes de moelle osseuse ?
Une étude de phase III a évalué l’impact de l’alimentation protégée au cours des greffes de moelle osseuse. Une alimentation protégée est utilisée par une majorité des centres de greffe de moelle (93%) sans preuve du bénéfice (diminution théorique des sources d’infection digestive mais pouvant impacter la qualité du microbiote intestinal) sachant qu’une alimentation protégée a été associée à un surrisque d’infection à Clostridium difficile (infection bactérienne sévère). Cette étude a été réalisée entrealimentation non restrictive pour 111 patients (tout autorisé sauf viandes et poissons crus) versus alimentation protégée pour 111 patients (nourriture cuite à plus de 80°C ou fruit pelé avec interdiction d’aliment cru de tout type [viande, poissons, légumes, fruit], des sauces, des yahourts et du miel). Seulement 20% de patients dans chaque bras ont été allogreffés, le reste étant des patients ayant reçu des autogreffes pour myélome ou lymphome. Il n’y apas de différence entre les 2 bras concernant le critère principal basé sur le taux d’infection. En revanche, il y a eu plus d’infections d’origine digestive et de perte de poids en alimentation protégée qu’en alimentation restrictive. Une amélioration des scores de qualité de vie a été observée dans le bras non restrictif par rapport au bras protecteur. Ces données nous font questionner nos prises en charge pour trouver le juste milieu dans la prise en charge diététique lors des procédures de greffe.
Comment évaluer le risque thrombotique artérielle et veineux dans les syndromes myéloprolifératifs ?
Pour finir dans un autre registre, Hélène Pasquer a présenté une étude sur le risque de thrombose, artérielle ou veineuse et les syndromes myéloprolifératifs (SMP) sur une cohorte de Saint Louis de 1055 patients. Les événements thrombotiques demeurent la principale complication des SMPet qui est responsable d’une morbi-mortalité. Avec un suivi médian de 10 ans, les patients ont présenté 75 thromboses artérielles et 97 thromboses veineuses avec très peu de patients (<5) présentant l’association des deux. Cette donnée clinique associée à des physiopathologies différentes ont fait proposer de différencier le risque de ces 2 types de thromboses, artérielles et veineuses afin d’établir un score prédictif. Les éléments retenus du score pour prédire la survenue d’un événement artérielle sont : un âge supérieur à 60 ans, un antécédent d’événement artériel, la présence de facteurs de risque cardio-vasculaires(tabac, diabète, antécédent familiaux de maladie cardio-vasculaire et hypercholestérolémie) et la présence d’une mutation de TET2 ou de DNMT3A. Ce score artériel permet d’obtenir des meilleurs résultats que les scores actuels proposés par European Leukemia Network (ELN). Les éléments retenus du score pour prédire la survenue d’un événement veineux sont uniquement un antécédent d’événement veineux et la présence d’une mutation JAK2V617F. A contrario, ce score est équivalent à celui proposé par l’ELN. Au total, des scores simples sont proposés pour estimer ces risques et après validation sur une autre cohorte, il pourrait aider à mieux prendre en charge les patients atteints de SMP sur le choix de traitement préventif de ces événements thrombotiques.
Article réalisé par Pierre-Edouard Debureaux, Interne en hématologie, Responsable Partenaires et ancien Président de l’Association des Internes en Hématologie (AIH).